患者さんの予後やQOL改善への”うま味”の臨床応用

演題:うま味研究と活用の最前線〜うま味を味方にする新しい栄養ケアのススメ〜
初出:2021年度 全国栄養士大会・オンライン
開催日・場所:2021年8月1日(日)〜31日(火)/オンライン
本講演では、まず味覚障害の実態に触れたいと思います。若くて健康だと思っている人でも味覚感度が低下している人が意外に多いという話です。続いて、その味覚の中で今、うま味が注目されていることについて。次に、我々が取り組んでいるうま味関連の研究、とくにがん患者さんの味覚障害に関する研究を紹介します。そして、がん患者さんだけでなく、高齢者を含め多くの方に対して、うま味を活用した栄養介入のメリットと、今後の展開についてお話しいたします。
あなたの近くにもいる隠れ味覚障害
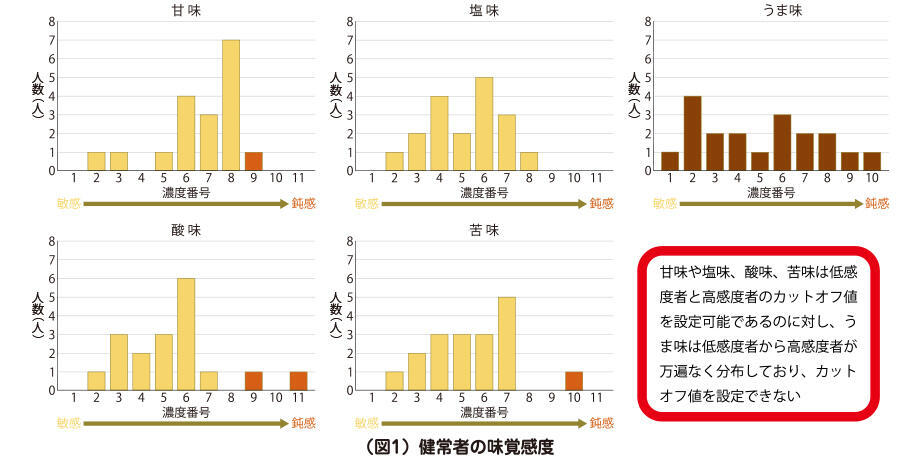
味覚障害の原因としてよく知られているのは亜鉛欠乏で、その他に薬剤性や心因性、原因を特定できない特発性などが多く、今では新型コロナウイルス感染症に伴う味覚障害が注目されています。 では、味覚の感度はどうなのかということで、我々も簡便なろ紙ディスク法や、判定精度に優れている全口腔法という手法で検討してみました。その結果、対象の17%の人が、基本五味のうちの甘味、塩味、酸味、苦味のいずれかが低下していました。一方、うま味に関しては、感度の低い人から高い人まで万遍なく分布していて、カットオフ値(判定値)を設定できないという結果でした (図1)。
そこで、うま味の感度が高い人と低い人を比較してみると、最も顕著な違いはBMIであり、うま味感度の低い人はBMI高値の人が多いことがわかりました。また、感度が低い人は食塩やアルコールの摂取量が多いのに比べて、野菜摂取量が少ない傾向にありました。
なぜうま味が注目されるのか?
よく知られているように、うま味は1908年に池田菊苗先生によって発見されたものの、世界的には長らく食品中の一成分に過ぎないと考えられていました。ところが2002年にうま味受容体が発見され、基本五味の一つとして位置づけられ、現在では全世界で「umami」として活用・研究されています。
日本人はうま味を”だしの味”と考えていますが、世界的には今「うま味=ヘルシー」と認識され注目されています。興味深いことに、うま味成分の一つであるグルタミン酸は母乳中にも含まれており、うま味はヒトが出生直後に味わう味覚と言うこともできます。
うま味がもつ数々のメリットについて話を進めていきますが、最初に取り上げるのはやはり、一番明快な「味をはっきりさせる」効果です。出汁をしっかりとることで、塩分を増やさずに味がしっかりします。うま味をたくさん使うと言うと、あたかも添加物を利用するかのようなイメージをもたれるかもしれませんが、実際には食べ物本来の味を引き出すということです。
では、我々はうま味をどのように感じているのでしょうか。かつては舌の先端で甘味を感じ、奥のほうで苦味を感じるといった感覚領域の分布が定説のように流布されていましたが、現在これは否定され、味蕾細胞は舌全体に分布し、とくに舌の奥に多く分布していることがわかっています。
味蕾は、前駆細胞の段階では酸味のみを感じることができますが、これはおそらく腐敗したものを吐き出す必要があるためだと考えられています。発育とともに味蕾細胞が成熟していき、また実際にさまざまな味の刺激を受けることで味覚が熟していきます。
日本人は味に繊細だと言われますが、和食は味がわずかに異なる多くの食材を使うため、そのような食生活が味蕾細胞の感度を高めているのではないかと考えられています。実際に、グルタミン酸を1日3g摂取することで、うま味や甘味の味覚受容体T1R3※1の発現が上昇すること、それに伴い、とくにふだんの食生活でのグルタミン酸の摂取量が少ない人ほど味覚感度が改善することが実験的にわかりました(図2)。
※1 T1R3:Taste Receptor Type 1 Member 3の略。うま味に対する味覚受容体

最期まで「おいしく」を支えるために
このような味覚刺激の効果を臨床に生かせないかということで、我々はさまざまな取り組みをしています。例えば外来化学療法室での栄養サポートです。外来化学療法中の患者さんの8割以上が副作用を訴えますが、その多くが栄養関連で、中でも食欲不振、体重減少、味覚障害が上位を占めます。
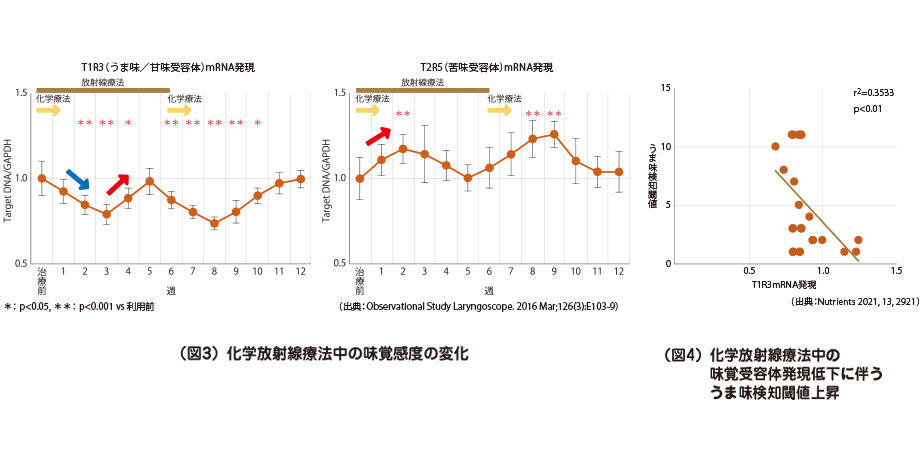
これらの副作用に対して、栄養士として何か役立てることはないかと試行錯誤を続けています。その中で、先ほどお話しした、うま味や甘味の受容体T1R3の発現が、化学放射線療法の開始とともに有意に低下することがわかりました(図3左)。その一方で、苦味の受容体であるT2R5は増加します(図3右)。また、T1R3の発現低下とともに、実際にうま味を検知する閾値が上昇することもわかりました(図4)。
患者さんが味覚異常を訴えても、これまでは「治療期間中だけですから」と説明して我慢してもらっていたのですが、治療終了後も十分に回復しないケースもありますし、体重減少はできるだけ抑制したいところです。そこで我々は、うま味を活用した食事介入を試みました。
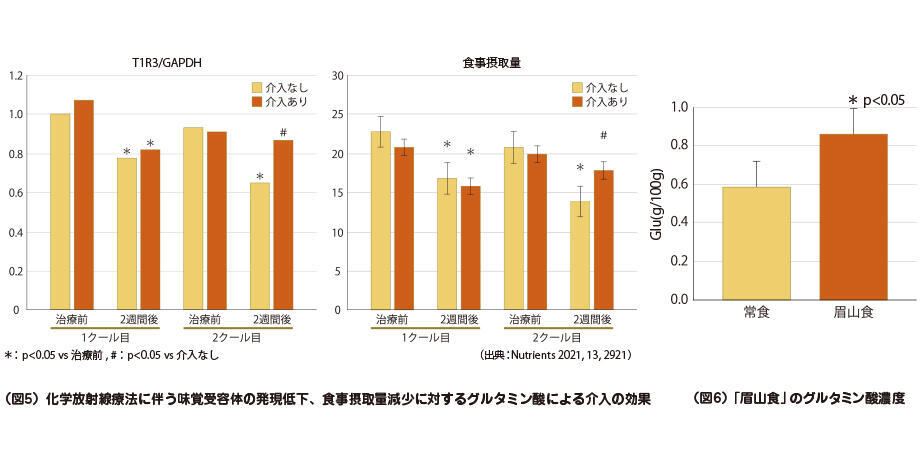
この介入の理論的根拠として、抗がん剤5-FUの投与でT1R3が減少するものの、グルタミン酸の摂取によってその減少が抑制されることを確認しています。その効果を患者さんにも期待できないかという研究です。結果は(図5)に示すように、2クール終了時点では介入なしの対照群に比較し有意にT1R3の発現と食事摂取量が多く、かつ化学療法施行前と有意差がみられませんでした。
ところで、我々がこのような科学的エビデンスを示すよりもずっと以前から、徳島大学病院には「眉山食」と呼ばれるがん患者さん向けの病院食が提供されています。眉山とは徳島市内にある山で、当地のシンボル的な存在です。
眉山食は、がん患者さんに何を食べたいかというアンケートを行い、その結果をフィードバックさせながら形づくられたものです。例えば焼きおむすびのだし茶漬け、だし巻卵、焼き茄子、フルーツの盛り合わせなどです。この眉山食の栄養成分を解析したところ、一般食に比べて有意にグルタミン酸を多く含んでいることがわかりました(図6)。この事実は、つらい状況にある患者さんはグルタミン酸の豊富な食事を求めていることの証しではないかと考えています。
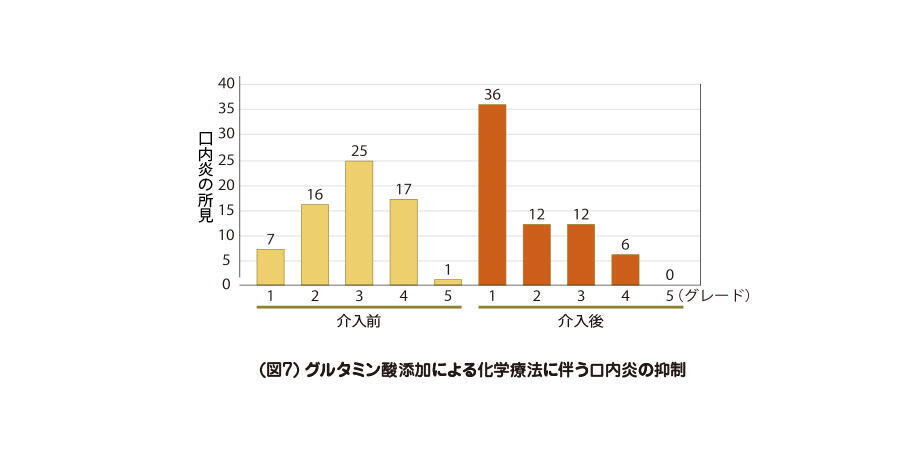
この研究を報告後、他院でも化学療法中の患者さんに対してグルタミン酸添加食が提供されるようになり、その中でさらにグルタミン酸介入により抗がん剤の副作用である口内炎が減ることもわかってきました(図7)。グルタミン酸による唾液分泌の促進や粘膜保護作用による効果と、我々は推察しています。
うま味を必要とするすべての人に
うま味のメリットを期待できるのはがん患者さんにとどまりません。現在は十文字学園女子大学の山本茂先生が徳島大にいらしたときのご研究では、認知症で食が進まず低栄養状態にある方の食事にグルタミン酸を添加したところ、食事量が増えただけでなく胆汁酸や胃酸の分泌も増え、さらに総リンパ球数の有意な増加がみられ栄養状態が改善したと報告されています1)。
また、味覚受容体の発現が口腔内細菌量と逆相関することも明らかになってきており、高齢者の疾病管理において味覚受容体を刺激することの有用性が期待されます。 高齢者以外では、肥満との関連が注目されています。うま味に対する感度を長年研究されている山陰労災病院の水田栄之助先生は昨年、うま味感度の低い人には肥満者が多いというデータを報告されました2)。その水田先生とともに我々もNHKの企画に加わり、20~70歳代の健康な方103人の味覚検査をさせていただきました。
その結果、肥満者に加え、痩せていて低栄養状態と考えられる人にも、うま味感度が低い人が多いことがわかりました。その他に、過去半年以内に体重が増加した人や喫煙者、早食いの人、多量飲酒者、うま味の基と言える肉や魚や乳製品などではなく嗜好品の摂取量が多い人も、うま味感度が低いことが示されました。
また、調味料として用いられるグルタミン酸ナトリウムは、名称に「ナトリウム」とついているため医療従事者からも「使いすぎると塩分過多になるのでは?」と質問を受けることがありますが、うま味がしっかりしてるほど塩分摂取量が減ることが知られていて、この研究でも漬物に醤油をかける人や塩味を控えようと心がけていない人のほうが、うま味感度が低いという結果でした。
うま味研究のこれからの展開と大活用術
味覚受容体は舌だけでなく、全身に発現していることも明らかになっています。ただ、その役割はほとんどわかっていません。
我々は胃の中の味覚受容体に注目しています。胃切除後に化学療法を行っていない患者さんにも、味覚障害が現れることが以前から知られており、それは胃の味覚受容体が失われたためではないかとの仮説の下、研究を進めています。
これまでのさまざまな研究から、とくに胃噴門部に味覚の受容体が多く、その受容体をグルタミン酸で刺激することによって発現が増加するという結果が得られています。また甘味による胃内のT1R1やT1R2の刺激により、インクレチンであるGLP-1の分泌が促進され、うま味による胃内のT1R3の刺激により、食欲亢進作用のあるグレリン分泌が促進される可能性が示されています。つまり、胃切除によって味覚を失うとともに、消化管ホルモンの適切な分泌刺激も失われてしまうのではないかと考えられます。
また我々は今、光るメダカを用いた研究も進めています(図8)。味覚受容体が刺激されると発光するため、動物を犠牲にせずに実験を繰り返すことができます。マウスに比して5倍も味蕾細胞が多い点も実験に適しています。この光るメダカを用いてさまざまな食品による味覚刺激を検討していますが、今のところ最も強く発光する成分はグルタミン酸であり、それを上回るものは見つかっていません。

これらのほかに、善玉アディポカインとして知られる脂肪細胞由来のアディポネクチンが唾液中にも分泌されていて、味覚受容体を介して認識され、抗肥満など何らかの作用を発揮している可能性が明らかになりつつあります。また、同じく脂肪細胞由来のレプチンは食欲抑制作用を持っていますが、肥満者ではT1R3の感度応答が低下し甘味を感じにくくなっている可能性もわかってきました。食欲と味覚受容体は密接な関係にあり、そのバランスが崩れることが代謝性疾患の進展と相互に関連している可能性があります。
私は味覚を、生涯の健康維持にかかわる要素だと捉えています。とくにうま味に関しては、本日紹介してきた研究からも、加齢よりもむしろ食生活との関連のほうが強いと言え、それだけ大きな介入効果を秘めていると期待できます。 うま味を用いた介入によって、子どもか高齢者か、経口摂取可能か否かにかかわらず、多くの人のQOLや疾患治療状態を改善させられる、さまざまな可能性があると考えています。
文献
- 1) Am J Clin Nutr. 2009 Sep;90(3):844S-849S
- 2) Hypertens Res. 2021 May;44(5):595-597
Profile

堤 理恵(つつみ りえ) 先生
徳島大学大学院医歯薬学研究部代謝栄養学分野講師。
管理栄養士・栄養学博士。専門は臨床栄養学(急性期医療栄養学)。
略歴
2001年 武庫川女子大学生活環境学部卒業
2006年 徳島大学大学院栄養学研究科博士後期課程修了
2005年 カリフォルニア大学サンディエゴ校医学部研究員
2008年 武庫川女子大学講師
2010年 徳島大学大学院・ヘルスバイオサイエンス研究部助教、現職に至る。
日本静脈経腸栄養学会評議員、日本病態栄養学会評 議員、日本小児栄養研究会理事、米国集中治療医学会 GI&Nutrition Award、米国内分泌学会 Top of Women Scientist、徳島県科学技術大賞。
